| 图片: | |
|---|---|
| 名称: | |
| 描述: | |
- 2014年第03期(总第82期)——大阴唇皮肤(已点评)
首先,结合本例,我们回顾复习一下V IN病理分类。历史上V IN的诊断一度缺乏统一的标准, 对于该类病变曾有多种不同命名, 包括外阴非典型增生、鲍温病( Bowen disease)、鲍温样丘疹病( Bowenoid papulosis)、Quera t增殖性红斑( Querat serythroplasia)、外阴单纯性原位癌。1986年, 国际外阴疾病学会( Internationa l Society for the study o f Vulvar Disease,ISSVD)建议统一使用外阴上皮内瘤样病变这一术语。并根据病变部位的细胞成熟度、核异型性、成熟障碍及有丝分裂活跃性分为V IN1-3级。此外, ISSVD在1986年还增加了一个分化型V IN 的定义, 将其也归于VIN3病变。
然而,与C IN 不同, 并无证据表明V IN 在病程中也是经历由VIN1至V IN3 的发展过程。此外, 近年来研究已证实, 外阴浸润癌存在有H PV感染相关型与HPV 感染不相关型两种不同类型, 它们在流行病学、临床表现、组织病理学以及分子生物学特性上均有所不同。相应地, 这两种不同类型的外阴浸润癌所对应的癌前病变V IN也分别为HPV感染相关型与H PV感染不相关型。因此, 2004年ISSVD对V IN分类定义进行了重新修正。VIN1定义不再使用, 新的V IN 定义仅指高级别V IN病变, 其中与HPV 感染相关者命名为普通型V IN( usual type), 并根据其病理表现进一步分为湿疣型( warty type), 基底细胞型( basaloid type ) 及混合型( mixed type); 与HPV 感染不相关者命名为分化型VIN(differentiated type);其他不能归入上述2类的V IN 病变归入未分类型VIN (unclassifiedtype)。
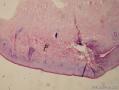
VIN巨检 病灶表现为表皮增生, 局部可有皮肤增厚斑块、乳头或小的赘疣, 表面可呈黑色素沉着、灰白色或暗红色。寻常型VIN多见为界限清晰的皮肤病损, 病变部位颜色与周围正常皮肤之间的界限清晰。外观可呈疣状或扁平样增生改变。分化型VIN 经常见于发生有硬化性苔藓或扁平苔藓的部位中, 可呈局部隆起状表现。
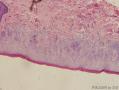
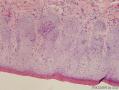
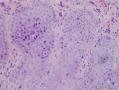
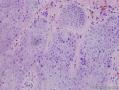
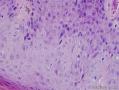
VIN镜检 被覆表皮增厚, 可形成乳头。表皮细胞极性紊乱, 细胞成熟不良, 可见核异常及核分裂相增加。湿疣型VIN镜下特征为湿疣状改变, 存在角化不全及角化过度, 细胞异型性明显; 多核细胞、圆形体、挖空细胞及细胞有丝分裂相多见。上皮棘层肥厚, 表皮网脊宽且深, 常可达上皮表面。表皮呈钉突样改变。基底细胞型V IN 病变特点为上皮层增厚且表面平坦, 表皮内见大量增殖的形态相对一致、呈现基底细胞样表现的未分化细胞从基底层向上扩展, 可达上皮全层; 圆形体及挖空细胞少于疣型V IN。混合型V IN病灶中兼有上述两种病理表现。分化型VIN 与H PV感染不相关, 镜下病理表现为细胞分化好, 细胞异型性局限于上皮基底层和靠近基底层的上皮区域, 或在这些部位最明显。基底细胞或基底旁细胞胞浆丰富, 有不良角化, 表皮网脊内常有角蛋白形成及角化珠样改变。IHC: P53(+), P16(-).因其细胞分化好, 并且少见有大范围的组织结构紊乱, 常常被混淆为良性病变。
本例综合分析,属于分化型VIN。
多数网友分析的都有一定道理,其中比较全面的首推23楼www810910 。

- If you have great talents, industry will improve them; if you have but moderate abilities, industry will supply their deficiency. 如果你很有天赋,勤勉会使其更加完美;如果你能力一般,勤勉会补足其缺陷。
诊断考虑:外阴白斑,上皮内瘤变VIN(高级别)。过去诊断名称还有:增生性营养不良,也有称外阴白色角化病的,诊断名称有些混乱。
诊断依据:1.临床上表现双大阴唇皮肤灰白、苔藓化,瘙痒;
2.病理表现:表皮角化不全,棘层肥厚增生,皮突下延增宽,多呈芽蕾状,表皮中下2/3层见增生活跃、排列紊乱、大小不一,部分核深染,并见少量角化不良细胞和病理性核分裂相。基底细胞无液化变性,真皮浅层血管周少至中量淋巴细胞、组织细胞浸润,少许噬色素细胞,胶原纤维未见明显变性;
3.免疫组化有较强的增值活性;
鉴别诊断:1.外阴硬化萎缩性苔藓:本病临床也可有外阴苔藓化、色素减退瘙痒表现,也可以不典型增生甚至癌变,但病史20余年多可见外阴皮肤萎缩,病理特点显示萎缩处角化过度、角化不全、表皮萎缩、基底细胞液化变性、真皮浅-中层胶原纤维均一化变性,不典型增生处显示表皮增生、异型,真皮胶原纤维尚可见变性,均与该患者不符,遂不考虑;
2.外阴慢性皮炎:无不典型增生,可排除。
l临床上习惯用外阴白色角化病
诊断考虑:外阴白斑,上皮内瘤变VIN(高级别)。过去诊断名称还有:增生性营养不良,也有称外阴白色角化病的,诊断名称有些混乱。
诊断依据:1.临床上表现双大阴唇皮肤灰白、苔藓化,瘙痒;
2.病理表现:表皮角化不全,棘层肥厚增生,皮突下延增宽,多呈芽蕾状,表皮中下2/3层见增生活跃、排列紊乱、大小不一,部分核深染,并见少量角化不良细胞和病理性核分裂相。基底细胞无液化变性,真皮浅层血管周少至中量淋巴细胞、组织细胞浸润,少许噬色素细胞,胶原纤维未见明显变性;
3.免疫组化有较强的增值活性;
鉴别诊断:1.外阴硬化萎缩性苔藓:本病临床也可有外阴苔藓化、色素减退瘙痒表现,也可以不典型增生甚至癌变,但病史20余年多可见外阴皮肤萎缩,病理特点显示萎缩处角化过度、角化不全、表皮萎缩、基底细胞液化变性、真皮浅-中层胶原纤维均一化变性,不典型增生处显示表皮增生、异型,真皮胶原纤维尚可见变性,均与该患者不符,遂不考虑;
2.外阴慢性皮炎:无不典型增生,可排除。
-
qiguaixiaozi 离线
- 帖子:147
- 粉蓝豆:16
- 经验:1821
- 注册时间:2011-01-12
- 加关注 | 发消息
-
lilyliu518 离线
- 帖子:31
- 粉蓝豆:15
- 经验:48
- 注册时间:2010-11-02
- 加关注 | 发消息
-
zyyzwangjin 离线
- 帖子:1220
- 粉蓝豆:262
- 经验:1873
- 注册时间:2013-08-19
- 加关注 | 发消息
诊 断:考虑分化型VIN(单纯性VIN)。
诊断依据:
1、临床及大体特征:分化型VIN较为少见,主要发生在老年妇女,病人症状明显,表现为外阴瘙痒或灼热感;其表现为单发或多发灰白色斑块,病变边界不清,表面粗糙。本例患者,女,71岁,外阴瘙痒20余年,近来加重。大体示双侧大阴唇皮肤粗糙、灰白,于病变显著部位取活检。
2、镜下特征:表皮增厚伴有角化不全,病变上皮由大的鳞状细胞组成,呈假上皮瘤样增生,异常的细胞出现在表皮的深层,越靠近基底层越明显,细胞胞浆丰富嗜酸性,可见细胞间桥,细胞核大呈空泡状,核仁明显,核分裂像易见。
3、免疫组化及HPV检测:可以帮助进一步确诊,HPV(-)、P16(-)、Ki-67(基底、副基底层+)、P53(+)。
鉴别诊断:
1、普通型VIN:免疫组化及HPV检测可以区别。
2、炎症反应性非典型增生:炎症较明显,无HPV感染证据。
3、硬化性苔藓:具有典型的特征,表皮萎缩变薄,上皮脚消失,有毛囊角栓形成,基底细胞液化变性。

选择
-
zq19931125 离线
- 帖子:681
- 粉蓝豆:4
- 经验:734
- 注册时间:2012-07-12
- 加关注 | 发消息
-
本帖最后由 www810910 于 2014-02-07 09:41:47 编辑
诊 断:考虑分化型VIN(单纯型VIN)。
诊断依据:
1、临床及大体特征:分化型VIN较为少见,主要发生在老年妇女,病人症状明显,表现为外阴瘙痒或灼热感;其表现为单发或多发灰白色斑块,病变边界不清,表面粗糙。本例患者,女,71岁,外阴瘙痒20余年,近来加重。大体示双侧大阴唇皮肤粗糙、灰白,于病变显著部位取活检。
2、镜下特征:表皮增厚伴有角化不全,病变上皮由大的鳞状细胞组成,呈假上皮瘤样增生,异常的细胞出现在表皮的深层,越靠近基底层越明显,细胞胞浆丰富嗜酸性,可见细胞间桥,细胞核大呈空泡状,核仁明显,核分裂像易见。
3、免疫组化及HPV检测:可以帮助进一步确诊,HPV(-)、P16(-)、Ki-67(基底、副基底层+)、P53(+)。
鉴别诊断:
1、普通型VIN:免疫组化及HPV检测可以区别。
2、炎症反应性非典型增生:炎症较明显,无HPV感染证据。
3、硬化性苔藓:具有典型的特征,表皮萎缩变薄,上皮脚消失,有毛囊角栓形成,基底细胞液化变性。
结合临床资料、镜下特征及免疫组化(Ki-67基底层副基底层+、p16-、p53灶性+),本例支持分化型VIN(单纯型VIN)的诊断。
在新一版的VIN分类中,VIN不再进行分级,而是进行了分型:即普通型(经典型)和分化型(单纯型)。因为VIN I多为一过性的HPV感染所致的外阴扁平湿疣,绝大多数经过治疗后可以恢复,将其放入外阴癌前期病变可能导致过治疗,因而不再将其归入VIN病变中;另外原分类中的VIN II和VIN III之间的病理诊断常有交叉,重复性很差,因而也不再区分,而是根据具体的病因及病理学改变进行分型(陈乐真老师《妇产科诊断病理学》第二版)。
分析不当之处尽请各位老师、同行批评指正!!

- 做人要知足,做事要知不足,做学问要不知足!
诊 断:考虑分化型VIN(单纯性VIN)。
诊断依据:
1、临床及大体特征:分化型VIN较为少见,主要发生在老年妇女,病人症状明显,表现为外阴瘙痒或灼热感;其表现为单发或多发灰白色斑块,病变边界不清,表面粗糙。本例患者,女,71岁,外阴瘙痒20余年,近来加重。大体示双侧大阴唇皮肤粗糙、灰白,于病变显著部位取活检。
2、镜下特征:表皮增厚伴有角化不全,病变上皮由大的鳞状细胞组成,呈假上皮瘤样增生,异常的细胞出现在表皮的深层,越靠近基底层越明显,细胞胞浆丰富嗜酸性,可见细胞间桥,细胞核大呈空泡状,核仁明显,核分裂像易见。
3、免疫组化及HPV检测:可以帮助进一步确诊,HPV(-)、P16(-)、Ki-67(基底、副基底层+)、P53(+)。
鉴别诊断:
1、普通型VIN:免疫组化及HPV检测可以区别。
2、炎症反应性非典型增生:炎症较明显,无HPV感染证据。
3、硬化性苔藓:具有典型的特征,表皮萎缩变薄,上皮脚消失,有毛囊角栓形成,基底细胞液化变性。

- 做人要知足,做事要知不足,做学问要不知足!