| 图片: | |
|---|---|
| 名称: | |
| 描述: | |
- 2015年第03期(总第111期)——右卵巢盆腹腔多发肿物(已点评)
| 性别 | 女 | 年龄 | 24 | 临床诊断 | 右卵巢盆腹腔多发肿物 |
|---|---|---|---|---|---|
| 一般病史 | 发现腹腔占位2天 | ||||
| 标本名称 | 卵巢、胃小弯、肠壁及子宫直肠窝 | ||||
| 大体所见 | 右卵巢肿物约2x2cm,于胃小弯肠壁及子宫直肠窝见广泛肿瘤种植,大者约10.0x10.0cm,小者约直径0.5cm. 2012年7月5日接到标本 2012年6约21日腹腔肿物穿刺:纤维组织,散在淋巴细胞浸润。 2012年6月18日行孕期检查时发现白细胞异常增高,骨髓穿刺:骨髓增殖性疾病(反应性?) | ||||
-
本帖最后由 草原 于 2017-09-25 22:26:42 编辑

- Stop walking today and you'll have to run tomorrow.
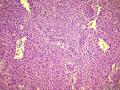
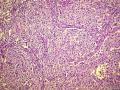
1.首先考虑淋巴造血系统肿瘤累犯卵巢:白血病或淋巴瘤可能性大。结合患者年龄及病史中提及2012年做过骨髓穿刺提示骨髓增殖性疾病可能。镜下特点:见肿瘤组织累犯卵巢皮质及髓质部分,并见尚有部分正常皮质残留。卵巢正常间质本身呈交叉席纹样排列方式。见肿瘤组织部分亦呈此种排列方式,其内见大小不等粘附性差的异型肿瘤细胞浸润,有些细胞呈小淋巴细胞样,部分血管壁内亦可见肿瘤细胞浸润。具体是什么类型白血病需依赖进一步免疫组化及结合临床血液病学进一步检查及流式结果确定。本人在工作过程中曾遇到一例白血病累犯卵巢。形态与此例十分相似。
2.还需考虑伴高钙血症的小细胞癌。
3.性索间质来源肿瘤需考虑
生殖细胞来源肿瘤形态学不像。不考虑。
感谢山东省肿瘤医院穆殿斌老师为有奖读片专栏提供病例!!!![]()

- Stop walking today and you'll have to run tomorrow.
-
本帖最后由 www810910 于 2015-04-03 21:30:14 编辑
诊 断:无性细胞瘤,伴腹腔、盆腔广泛种植性转移。
诊断依据:
(1)临床资料:患者,女,24岁,发现腹腔占位2天,临床诊断“右卵巢、盆腹腔多发肿物”。
(2)大体检查:送检卵巢、胃小弯、肠壁及子宫直肠窝肿物,右卵巢肿物约2x
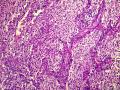
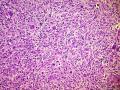
(3)镜下观察:低倍镜示卵巢实质内境界相对清楚的实性肿物,局部血管扩张充血、实质出血;肿瘤细胞呈实性片状、巢状分布,局部似乎形成腺腔结构,肿瘤细胞密集,其间可见部分梭形细胞及散在的淋巴细胞浸润;高倍镜示肿瘤细胞为较一致的圆形、多边形,细胞界限较清,胞浆丰富淡染或弱嗜酸,细胞核呈圆形、卵圆形,居中,核膜较清楚、增厚且不规则,染色质呈颗粒状,可见明显的核仁;局部可见多核瘤巨细胞;可见核分裂象。
免疫组化:PLAP、CD117、D2-40、OCT4、CK、EMA、NSE、AFP等。
鉴别诊断:
(1)原始生殖细胞肿瘤(胚胎癌和卵黄囊瘤):胚胎性癌细胞异型显著,卵黄囊瘤有S-D小体,免疫组化AFP有助于鉴别诊断;
(2)透明细胞癌:无性细胞瘤患者年龄<30岁,透明细胞癌患者多为绝经前后;
(3)小细胞未分化癌,高血钙型:其多伴有分泌性高钙血症相关的一些临床症状,免疫组化CK、EMA等有助于鉴别诊断。
以上纯属己见,分析不当的地方敬请各位老师、同行批评指正!
-
snowman103cn: 年纪这么轻,先把癌全排除了,生殖里哪一型都放不进, 按发病率来算,当然是淋巴-造血系排前面了2015-04-30 21:39
-
www810910: 谢谢老师指导……2015-04-30 22:34

- 做人要知足,做事要知不足,做学问要不知足!
-
qiguaixiaozi 离线
- 帖子:147
- 粉蓝豆:16
- 经验:1821
- 注册时间:2011-01-12
- 加关注 | 发消息
考虑间变性大细胞淋巴瘤,肉瘤样型
1.患者,年轻,24岁,多发性肿物,出现白细胞异常增高;2.片状排列、席纹状排列,瘤细胞胖梭形、卵圆形及多边形,上皮样,核大,核圆、卵圆,核膜不规则,有小核仁,可见多核巨细胞及核分裂象,胞浆较丰富,嗜酸性,部分透明,间质多量淋巴细胞、浆细胞浸润,血管增多,内皮细胞增生明显;
鉴别:上皮样炎性肌纤维母细胞肉瘤、恶性中胚叶混合瘤、胃肠道间质瘤、上皮样PEComa等。
5楼说得有道理。但我首选:滤泡树突状细胞肉瘤/FDCS或交指状突细胞肉瘤/IDCS(形态学难以区分,只能靠免疫组化,前者远多见于后者),主要是肥胖梭形、上皮样、多形性的细胞和炎症背景相混杂。有片状、结节状、束状、漩涡状结构,这些是FDCS或IDCS的典型特征。鉴别诊断炎性肌纤维母细胞肉瘤(这里的炎性肌纤维母细胞肉瘤/IMFS不同于我们常说的炎性肌纤维母细胞瘤IMT,要更加具有侵袭性),但大多好发于胃肠道。IMFS弥漫强表达desmin和ALK、CD30,形态上-上皮样的细胞更像肥胖的核偏位的神经节细胞。由于免疫组化和间变大细胞淋巴瘤的部分重叠,所以要排除间变大细胞淋巴瘤,但Desmin(+++)能排除肉瘤样型的间变大细胞淋巴瘤
-
snowman103cn: 要我就首选大间变,排除一下FDC肉瘤/组织细胞肉瘤 和你颠倒一下2015-04-30 21:23
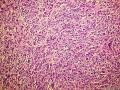
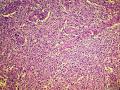
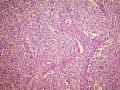
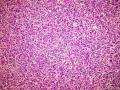
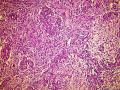
该病例的形态特点是:肿瘤由卵圆形至短梭形的瘤细胞和混杂的大量小淋巴细胞、浆细胞及分叶核细胞组成。肿瘤细胞多呈片状或交织的条索状排列,可见明显的席纹状结构。部分肿瘤内血管丰富,血管内皮增生明显。肿瘤部分区域可见扩张的假血管性裂隙,内含淡嗜伊红色的蛋白样液体。小淋巴细胞散在或倾向于聚集在血管周围,形成套袖样结构。高倍镜下,瘤细胞的边界不清楚,核呈圆形、卵圆形或短梭形,核膜清晰,核仁不明显或见小核仁,染色质透亮、空泡状或点彩状。局灶区域还可见分叶状或多核瘤细胞。
免疫组化结果:CD21+、 CD23+、 CD35+、 Vimentin+、 CD30+、 EMA弱+、 CD68散在+、 S-100-、 LCA-、 CD20-、 CD3-、 CD117-、 CD34-、CKp-、 CAM5.2-、 CK5/6-、 CR-、 HHF-35-、PLAP-、α-Inhibin-、AFP-
最后病理诊断:滤泡树突细胞肿瘤/肉瘤。
讨论:滤泡树突细胞肿瘤/肉瘤发病年龄14~77岁,平均47岁。男女比例相当,或女性略多见。发病部位多数位于淋巴结内,发生在淋巴结内的病例约占所有病例的1/2至2/3,其中以颈部及腋窝淋巴结最常累及。结外多个部位也可发生,包括肝、脾、扁桃体、小肠及其系膜、纵膈、腹膜后、颈部软组织、口腔、腮腺、甲状腺、胸肺、胃肠道、皮肤、甚至乳腺等。临床表现为无痛性缓慢生长的界限清楚的肿块,发生于腹腔内的FDCS可出现腹痛、腹部包块或消化道症状,全身症状一般不明显。
病理形态学方面,肿瘤大小与发生部位有关,位于头颈部及浅表部位体积相对较小。位于腹腔、腹膜后及纵膈等深部组织者,一般体积较大。低倍镜下:肿瘤细胞呈梭形或卵圆形,有时呈上皮样,显示特征性的双相型细胞形态,瘤细胞多呈片状、交织状或席纹状排列,在部分肿瘤内可见呈同心圆状的旋涡样结构,类似脑膜瘤。肿瘤组织内常混杂有大量小淋巴细胞或浆细胞。部分肿瘤内血管比较明显,少数病例内可见扩张的假血管性裂隙,内含淡嗜伊红色的蛋白样液体,加上倾向于聚集在血管周围的小淋巴细胞所形成的套袖样结构,类似胸腺瘤。高倍镜下,瘤细胞边界不清楚常呈合体细胞样,核卵圆形、圆形或梭形,核膜清晰,核仁小或不明显,染色质空泡状或点彩状,核内有时可见假包涵体,局灶区域还可见分叶状或多核瘤巨细胞,后者类似Warthin-Finkeldy巨细胞。瘤细胞的异型性和核分裂象在病例之间差异较大,多数病例细胞学特征温和,核分裂1~35个/10HPF。一些体积较大的肿瘤内可见灶状、片状或地图样凝固性坏死。发生于淋巴结内或结外的FDCS形态相似,但发生于肝脾的FDCS与其他部位有所不同,组织形态上常类似炎性假瘤,Cheuk等将其描述为炎性假瘤样FDCS。
免疫表型特征,FDCS免疫表型与正常FDC基本一致,CD21、CD35是目前诊断FDCS经典的、最常用的特异性抗体,R4/23、Ki-M4、Ki-FDC1也是特异性很强的抗体,部分病例还可表达Vimentin、CD68、S-100蛋白、EMA、SMA等。近年来发现的一些新抗体可能在FDCS的诊断中起到重要作用,比如:fascin蛋白、CXCL-13、clusterin等。值得一提的是clusterin,其在FDCS中强烈而弥漫的表达可以与指突状树突细胞肿瘤、朗格汉斯细胞肿瘤相鉴别,而且某些不表达CD21、CD23、CD35的FDCS病例也可表达clusterin。除此之外,本病例还发现,肿瘤细胞对CD30呈阳性表达,这在以往文献中未见报道,由于病例太少,其意义还有待于观察。
鉴别诊断,FDCS是一种比较罕见的肿瘤,其组织结构与其他许多肿瘤有相似之处,而且形态变化也较大,因此易与其他肿瘤相混淆,比如:朗格汉斯细胞肿瘤、指状突树突细胞肿瘤、炎性假瘤/炎性肌纤维母细胞瘤、恶性外周神经鞘瘤、恶性纤维组织细胞瘤、淋巴上皮癌、胸腺瘤等等。发生在腹腔的FDCS尤其注意与恶性胃肠道间质瘤和腹膜间皮肉瘤等相鉴别。
本人遇到的几例结外FDCs,包括本例,都没有在一开始就诊断本病。本例应该说形态比较典型,但很多网友也没有想到本病,可见其诊断的困难性。本人的经验是,不怕做不到,就怕想不到,提高警惕是防止误诊的关键,无论在什么部位,如果肿瘤具有以下形态特点时都要想到本病:细胞呈卵圆形至梭形,有时呈上皮样,显示双相型形态;呈片状、交织状或席纹状排列,肿瘤组织内混杂有大量小淋巴细胞或浆细胞。
免疫组化标记对于鉴别诊断有重要作用。

- 博学之,审问之,慎思之,明辨之,笃行之。
-
bingliwang 离线
- 帖子:81
- 粉蓝豆:514
- 经验:639
- 注册时间:2006-11-13
- 加关注 | 发消息
滤泡树突状肉瘤(低级别)
诊断要点:
1、广泛累计腹腔,有淋巴造血指标异常
2、结构有围血管炎细胞聚集,组织样细胞呈片状、结节状、束状、漩涡状结构;
3、细胞肥胖梭形、上皮样、多形性的细胞和炎症背景相混杂;及
4、加做免疫组化CD21\CD35\CD23等
鉴别诊断:
组织细胞肉瘤、粒细胞肉瘤等其他淋巴造血肿瘤,软组织肿瘤。形态学特征及免疫组化可鉴别。

- 病理观片法重要,法不精通脖架刀; 先用低倍后用高,弄清结构弄细胞; 实质下落间质飘,背景当中向外挑; 细胞源性快寻到,思维开阔勿担稍; 免疫组化常用到,前沿科技不可少; 千形万态慎思考,留有余地更重要。
-
本帖最后由 清秋 于 2015-06-17 11:09:25 编辑
滤泡树突细胞肉瘤是一类形态学呈梭形或椭圆形的细胞和表型上呈现滤泡树突细胞特征的肿瘤性增殖。病因不明,是少见的肿瘤,年龄分布广泛,多数是成人,男女性别相当。颈部淋巴结是最常发生的部位,其他结外的多个部位也可发生,患者多表现为缓慢生长的无痛性肿块,肿瘤细胞普遍表达非肿瘤滤泡树突细胞的表型,生物学行为惰性,更像低度恶性的肉瘤。多数可手术切除干净。40%~50%的病例出现局部复发。
学习!

- 快乐学习!认真工作
-
wanghuifang 离线
- 帖子:11
- 粉蓝豆:0
- 经验:137
- 注册时间:2013-02-18
- 加关注 | 发消息